Методы титриметрического анализа
В зависимости от типа применяемой реакции методы титриметрических определений делятся на четыре группы.
1. Метод нейтрализации. Кислотно-основное титрование, основанное на реакции нейтрализации:
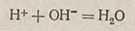
Применяется для определения кислот и щелочей, а также слабых кислот и слабых оснований.
2. Методы редоксиметрии. Редокс-методы, основанные на реакциях окисления - восстановления. Широко применяются для определения многих катионов, анионов и ряда органических веществ. К редокс-методам относятся: перманганатометрия, йодометрия, дихроматометрия, броматометрия, ванадатометрия, титанометрия, меркурометрия и др.
3. Методы осаждения. Основаны на реакциях количественного осаждения определяемого иона. Наиболее широко применяются для определения анионов галогенов и ионов серебра: аргентометрия, роданометрия.
4. Методы комплексометрии. Основаны на образовании растворимых комплексных соединений ионов металлов с органическими реактивами (например, с ЭДТА) или с неорганическими анионами. Комплексометрически определяют также жесткость воды.
Общие приемы титрования
Прямое титрование. Простейший прием титрования состоит в том, что к определенному объему анализируемого раствора по каплям приливают из точно калиброванной бюретки стандартный (титрованный) раствор реагента. Титрование ведут до точки эквивалентности, которую определяют визуально по изменению окраски раствора.
Обратное титрование. В тех случаях, когда прямое титрование по тем или иным причинам невозможно, применяют обратное титрование. Этот прием состоит в том, что к определенному объему анализируемого раствора приливают в избытке точно измеренный объем титрованного раствора реагента. Затем этот избыток оттитровывают стандартным раствором другого реагента.
Титрование заместителя. Некоторые катионы нельзя определять прямым титрованием, поскольку отсутствует подходящий индикатор или ион в условиях титрования подвергается гидролизу. В этих случаях используют титрование заместителя. Сущность этого приема титрования заключается в том, что к определяемому веществу прибавляют какой-либо вспомогательный реагент, реагирующий с этим веществом с выделением эквивалентного количества нового вещества, которое оттитровывают стандартным раствором основного реагента.
